KT综合征的临床认知与突破
2025-10-14 15:45
阅读:6713
来源:爱爱医
作者:谢宁
责任编辑:点滴管
[导读] 尽管KT综合征早在1900年就被法国医生Klippel和Trenaunay描述并命名,但百余年来,其本质始终是医学界争论的焦点:它究竟是一种先天性血管畸形,还是一种涉及血管、淋巴管、骨骼肌肉甚至基因调控的复杂系统性疾病?
引言:当“葡萄酒色斑”遇见“肢体肥大”——一个被低估的复杂疾病。
在血管外科或儿科门诊中,常有家长带着这样的孩子前来就诊:“医生,我家孩子出生时左腿就有一块红斑,当时以为是胎记,但现在他5岁了,左腿明显比右腿粗了一圈,还总说腿疼,走路有点跛……” 这类以“葡萄酒色斑(鲜红斑痣)+肢体肥大+浅静脉曲张”三联征为核心表现的疾病,正是临床中相对罕见却极易误诊的KT综合征(Klippel-Trenaunay Syndrome,KTS)。
尽管KT综合征早在1900年就被法国医生Klippel和Trenaunay描述并命名,但百余年来,其本质始终是医学界争论的焦点:它究竟是一种先天性血管畸形,还是一种涉及血管、淋巴管、骨骼肌肉甚至基因调控的复杂系统性疾病?其核心病理机制是静脉发育异常、淋巴管缺如,还是动静脉瘘的隐匿参与?更关键的是,面对患者差异极大的临床表现(从轻微红斑到严重肢体功能障碍),现有的诊疗策略能否真正实现“精准干预”而非“过度治疗”?
本文将基于临床一线的真实观察,结合近年病理研究、影像学进展及多学科诊疗(MDT)实践,深入探讨KT综合征的认知演变、争议焦点与临床决策困境,试图为这一“古老而陌生”的疾病提供更贴近实际的学术思考。
一、KT综合征的本质争议:从“单纯血管畸形”到“系统发育异常”的范式转换
(一)传统认知:血管畸形的“经典三联征”
长期以来,KT综合征被归类为“先天性静脉畸形骨肥大综合征”,其典型表现为三联征:
① 葡萄酒色斑(鲜红斑痣):多为单侧肢体(95%以上累及下肢)的红色或紫红色斑片,出生即存在,按压不褪色,随年龄增长可能增厚或结节化。
② 肢体肥大:患侧肢体周径增粗(软组织增生)、骨骼增长(骨骺过度刺激),导致双侧肢体不对称(差异可达2-5cm甚至更显著)。
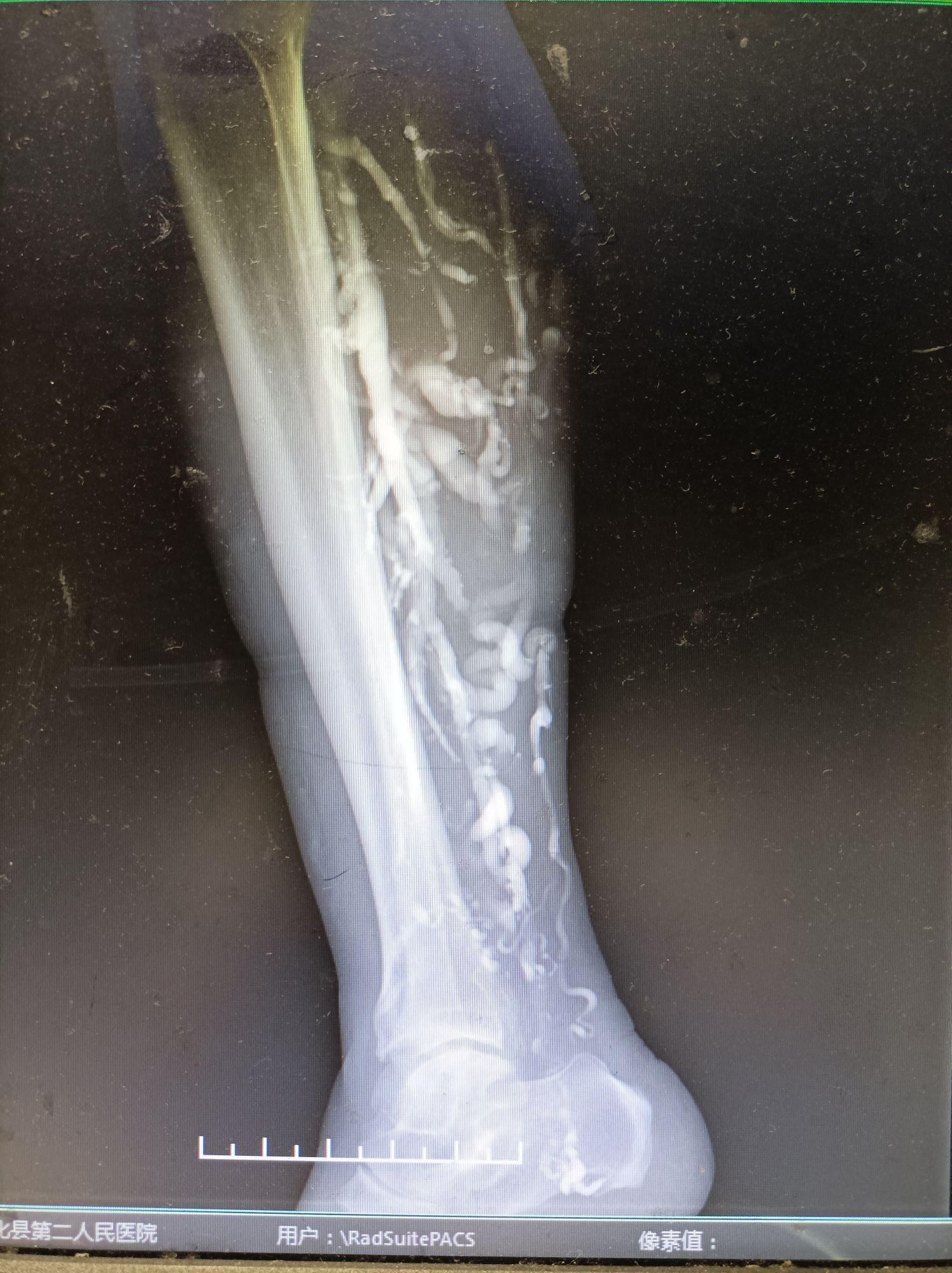
③ 浅静脉曲张:患肢浅表静脉迂曲扩张(多位于大腿外侧或小腿后方),部分患者合并深静脉发育不良或缺如。
这一经典描述曾长期主导临床思维——KT综合征被视为一种以静脉系统发育异常为核心的“局部血管畸形”,治疗重点自然落在“纠正静脉回流障碍”上(如硬化剂注射曲张静脉、手术切除畸形静脉团)。
(二)现代挑战:多系统受累的“隐藏真相”
随着病理学研究和临床随访的深入,传统认知的局限性逐渐暴露:
淋巴系统的“沉默缺位”:约60%-70%的KT患者存在淋巴管发育异常(如淋巴管数量减少、瓣膜功能不全),但常规超声或MRI难以直接显示。这些患者常合并反复淋巴水肿(肢体肿胀加重)、皮肤增厚(象皮肿样改变)或乳糜性胸腹水(淋巴管瘘),却被传统三联征的框架忽略。
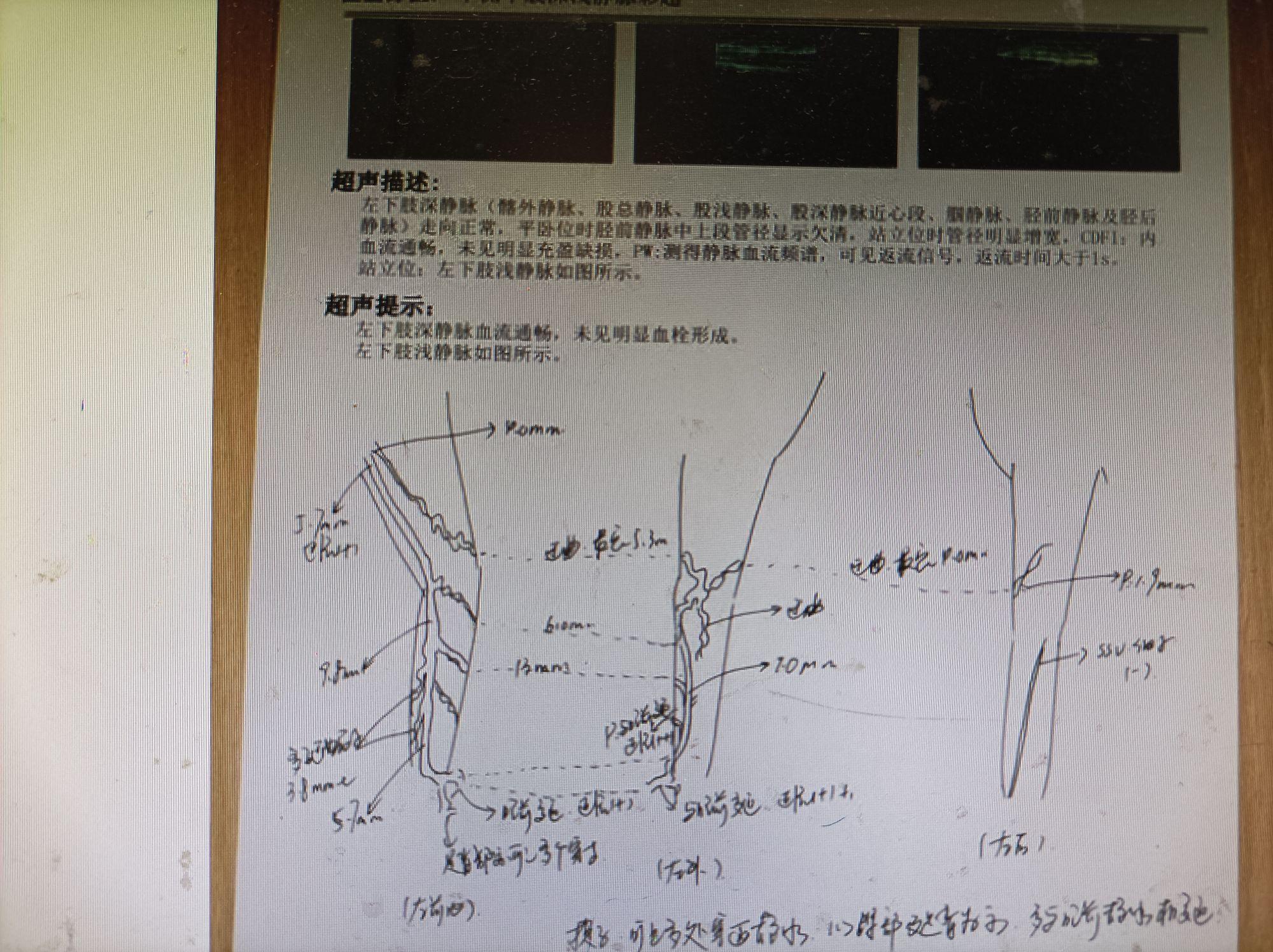
深静脉系统的“隐匿病变”:约30%-50%的KT患者存在深静脉发育不良(如股静脉缺如、髂静脉狭窄)或功能性梗阻(瓣膜功能不全),而非单纯的浅静脉扩张。这类患者若仅处理浅静脉曲张,可能因深静脉回流未改善导致症状复发甚至加重。
骨骼肌肉系统的“动态失衡”:肢体肥大不仅是软组织增生,更伴随骨骺过度刺激(患侧下肢骨生长速度比健侧快1.5-2倍),导致骨骼畸形(如胫骨弯曲、足弓塌陷)、关节负荷不均(膝踝关节炎发生率高达40%)及步态异常。
基因层面的“潜在调控异常”:近年研究发现,部分KT患者存在PIK3CA基因体细胞突变(约占30%-50%),该基因参与血管内皮生长因子(VEGF)信号通路调控,可能解释了血管/淋巴管异常增生的共同机制——但并非所有患者均携带该突变,提示KT可能是“多基因+环境因素”共同作用的结果。
二、诊断困境:当“典型表现”遇上“个体差异”
(一)临床分型的混乱与争议
目前国际上对KT综合征尚无统一的分型标准,常见的分类方式包括:
按血管异常主导类型分型:静脉型(以浅/深静脉发育异常为主)、淋巴-静脉型(合并淋巴管缺如)、动静脉瘘型(罕见,但可能导致严重高流量动静脉分流)。
按肢体受累范围分型:局限性(仅下肢局部受累)、弥漫性(整肢或双下肢受累)。
按并发症主导分型:以疼痛/肿胀为主、以肢体功能障碍为主、以皮肤溃疡/出血为主。
(二)诊断技术的“盲区”与互补需求
目前KT综合征的诊断依赖“临床三联征+影像学验证”,但每种技术均有其局限性:
超声检查:是首选的初筛工具,可显示浅静脉曲张、深静脉发育异常(如缺如、狭窄)及部分淋巴管扩张,但对深层结构(如骨骺生长板受刺激情况)及微小淋巴管缺如的分辨率不足;
MRI/MRA:能清晰显示软组织增生、骨骼长度差异及深静脉走行,但对淋巴管的直接成像仍依赖间接征象(如皮下组织增厚伴信号异常),且检查时间长、儿童配合度低。
淋巴造影:理论上可直观评估淋巴管通畅性,但因有创性(需注射造影剂至皮内淋巴管)和并发症风险(感染、过敏),临床极少常规开展。
基因检测:PIK3CA突变检测(通过皮肤活检或外周血)对部分患者有提示意义,但阴性结果不能排除KT综合征(约50%患者无该突变),且检测成本高、普及率低。
更棘手的是,许多基层医院因缺乏经验,常将KT综合征误诊为“单纯鲜红斑痣”(忽略肢体肥大)、“下肢静脉曲张”(忽略红斑和骨骼异常)或“淋巴水肿”(忽略血管畸形)。笔者曾接诊过一例12岁患儿,外院因“左小腿静脉曲张”行硬化剂治疗,术后出现皮肤溃疡——进一步检查才发现其自幼存在左下肢红斑和轻度肥大,实为KT综合征合并深静脉发育不良,硬化剂治疗反而加重了回流障碍。
三、治疗争议:从“对症治疗”到“系统管理”的艰难平衡
(一)核心矛盾:治疗目标的不统一
KT综合征的治疗目标究竟是什么?不同学科的医生存在显著分歧:
血管外科医生可能优先考虑“消除静脉曲张”(预防血栓或出血)。
骨科医生关注“矫正骨骼畸形”(改善步态和关节功能)。
皮肤科医生聚焦“红斑的美观问题”(激光治疗鲜红斑痣)。
患者家属则最关心“肢体不对称是否影响孩子心理”或“未来能否正常运动”。
这种目标的分散性导致治疗策略常陷入“头痛医头”的困境——例如,单纯硬化剂注射曲张静脉可能因深静脉回流未改善而复发;过早进行骨骼矫形手术可能因肢体持续生长导致畸形复发;激光治疗红斑虽能改善外观,但对肢体肥大或疼痛无任何帮助。
(二)具体治疗手段的争议与实践反思
1. 静脉异常的处理:从“盲目干预”到“功能评估优先”
传统观点认为,KT综合征的静脉曲张需早期干预(如硬化剂注射、手术剥脱),但近年研究发现:部分患者的浅静脉曲张是代偿性表现(因深静脉发育不良导致静脉血回流至浅静脉系统)——若盲目闭合浅静脉,可能反而加重深静脉负荷,导致肢体肿胀加剧。
目前的共识是:
先通过影像学(如静脉造影、MRV)明确深静脉功能状态,再决定是否处理浅静脉:
若深静脉通畅(如股静脉直径正常、血流速度达标),浅静脉曲张可考虑硬化剂或微创手术。
若深静脉缺如或严重狭窄,则需优先解决深静脉问题(如通过介入球囊扩张或搭桥手术)。再评估浅静脉处理必要性:
对于无症状的轻度静脉曲张(仅影响外观),可暂不干预,避免过度治疗。
2. 淋巴系统的“隐形干预”:被忽视的关键环节
约60%的KT患者存在淋巴回流障碍(尽管未表现出明显水肿),这类患者若仅处理静脉问题,肢体肿胀可能持续进展。但目前淋巴系统的治疗手段极为有限:
保守治疗:弹力袜/弹力绷带(压迫浅静脉和部分淋巴管)、淋巴引流按摩(需专业康复师指导)。
手术干预:如淋巴管-静脉吻合术(适用于淋巴管缺如但邻近静脉功能正常的患者),但因技术难度高、远期效果不确定,仅少数中心开展。
新兴探索:间充质干细胞注射(促进淋巴管再生)或基因靶向治疗(针对PIK3CA突变调控淋巴管发育),目前仍处于动物实验或小样本临床研究阶段。
临床实践中,我们常建议患者长期佩戴定制弹力袜(从儿童期开始),虽不能逆转淋巴管缺如,但能显著延缓肿胀进展——一位坚持佩戴10年的成年患者坦言:“如果不穿袜子,下午腿会比早上粗3cm,走路像灌了铅;但穿了袜子,至少能正常上班。”
3. 骨骼肌肉问题的“生长管理”:时机比手术更重要
肢体肥大伴随的骨骼过度生长是KT综合征最棘手的并发症之一。儿童期若不干预,可能导致双下肢长度差异超过5cm(严重影响行走),甚至继发脊柱侧弯。传统解决方案包括:
短缩健侧肢体(通过骨骺阻滞术限制健侧生长)。
延长患侧肢体(通过外固定支架牵拉骨骼,但手术创伤大、并发症多)。
观察等待(对于差异<2cm的患儿,通过鞋垫垫高平衡步态)。
但目前尚无绝对最优策略——短缩健侧可能影响整体身高发育;延长患侧需多次手术且存在感染/骨不连风险;而单纯观察可能导致患儿因步态异常产生心理问题。笔者的经验是:建立“骨骼生长监测档案”(每6个月测量双下肢长度、评估步态),在差异达到3cm前制定个性化方案(如差异2-3cm时优先定制矫形鞋垫,差异>3cm且年龄>8岁考虑骨骺阻滞术)。
4. 皮肤病变与并发症的“细节管理”:容易被低估的问题
鲜红斑痣在KT综合征患者中常伴随增厚或结节化(成年后发生率约20%),可能因摩擦导致出血或溃疡;浅静脉曲张严重者可能出现皮肤色素沉着、脂溢性皮炎甚至慢性溃疡。这类问题虽不致命,却显著影响生活质量——一位25岁的患者因小腿红斑结节反复破溃,最终发展为慢性骨髓炎,不得不接受局部皮瓣移植。
四、未来方向:从“经验性治疗”到“精准医学”的突破可能
(一)PIK3CA基因相关治疗的探索
约30%-50%的KT综合征患者携带体细胞PIK3CA突变(主要位于热点区域如E542K、E545K),该基因通过激活VEGF信号通路促进血管/淋巴管异常增生。针对这一靶点的靶向药物(如阿培利司,原用于乳腺癌PIK3CA突变治疗)已在国外开展小样本临床试验——初步结果显示,局部外用PIK3CA抑制剂可缩小部分患者的血管畸形范围,但全身用药的安全性(如高血糖、腹泻等副作用)仍需验证。
未来若能通过无创检测(如皮肤活检或液体活检)明确患者是否携带PIK3CA突变,并针对性应用靶向治疗,可能为KT综合征提供“对因干预”的新思路。
(二)患者教育与长期管理的科普缺失
许多KT综合征患者因“不致命”而被忽视——家长认为“胎记不用治”,患者觉得“腿粗点不影响生活”。但实际上,未规范管理的KT综合征可能导致成年后慢性疼痛、深静脉血栓甚至截肢风险增加。未来需加强基层医生的识别能力(如通过典型三联征早期筛查),并通过科普宣传让患者理解“早期干预”的意义(如儿童期佩戴弹力袜可延缓骨骼畸形)。
结语:KT综合征的诊疗启示——医学的复杂性在于“看见具体的患者”
KT综合征的百年认知史,本质上是一场从“局部表型”到“系统本质”的探索之旅。它提醒我们:临床医学中那些看似“典型”的疾病,往往隐藏着更复杂的真相——一条红斑下的静脉异常,可能牵连淋巴管、骨骼、基因甚至患者的心理健康;一套标准化的诊疗指南,永远无法覆盖每个患者的独特需求。
作为医生,我们或许无法立刻攻克KT综合征的所有难题,但至少可以做到:不再用“单纯血管畸形”的标签简化患者的痛苦,不再用“典型三联征”的框架限制诊断的视野,而是在每一次查房、每一次影像解读、每一次治疗决策中,看见那个具体的、有血有肉的患者——他可能只是希望腿不那么疼,能和同学一起跑操;她可能只想穿一条短裙,不用遮掩腿上的红斑。这,才是医学最本真的意义。
在血管外科或儿科门诊中,常有家长带着这样的孩子前来就诊:“医生,我家孩子出生时左腿就有一块红斑,当时以为是胎记,但现在他5岁了,左腿明显比右腿粗了一圈,还总说腿疼,走路有点跛……” 这类以“葡萄酒色斑(鲜红斑痣)+肢体肥大+浅静脉曲张”三联征为核心表现的疾病,正是临床中相对罕见却极易误诊的KT综合征(Klippel-Trenaunay Syndrome,KTS)。
尽管KT综合征早在1900年就被法国医生Klippel和Trenaunay描述并命名,但百余年来,其本质始终是医学界争论的焦点:它究竟是一种先天性血管畸形,还是一种涉及血管、淋巴管、骨骼肌肉甚至基因调控的复杂系统性疾病?其核心病理机制是静脉发育异常、淋巴管缺如,还是动静脉瘘的隐匿参与?更关键的是,面对患者差异极大的临床表现(从轻微红斑到严重肢体功能障碍),现有的诊疗策略能否真正实现“精准干预”而非“过度治疗”?
本文将基于临床一线的真实观察,结合近年病理研究、影像学进展及多学科诊疗(MDT)实践,深入探讨KT综合征的认知演变、争议焦点与临床决策困境,试图为这一“古老而陌生”的疾病提供更贴近实际的学术思考。
一、KT综合征的本质争议:从“单纯血管畸形”到“系统发育异常”的范式转换
(一)传统认知:血管畸形的“经典三联征”
长期以来,KT综合征被归类为“先天性静脉畸形骨肥大综合征”,其典型表现为三联征:
① 葡萄酒色斑(鲜红斑痣):多为单侧肢体(95%以上累及下肢)的红色或紫红色斑片,出生即存在,按压不褪色,随年龄增长可能增厚或结节化。
② 肢体肥大:患侧肢体周径增粗(软组织增生)、骨骼增长(骨骺过度刺激),导致双侧肢体不对称(差异可达2-5cm甚至更显著)。
③ 浅静脉曲张:患肢浅表静脉迂曲扩张(多位于大腿外侧或小腿后方),部分患者合并深静脉发育不良或缺如。
这一经典描述曾长期主导临床思维——KT综合征被视为一种以静脉系统发育异常为核心的“局部血管畸形”,治疗重点自然落在“纠正静脉回流障碍”上(如硬化剂注射曲张静脉、手术切除畸形静脉团)。
(二)现代挑战:多系统受累的“隐藏真相”
随着病理学研究和临床随访的深入,传统认知的局限性逐渐暴露:
淋巴系统的“沉默缺位”:约60%-70%的KT患者存在淋巴管发育异常(如淋巴管数量减少、瓣膜功能不全),但常规超声或MRI难以直接显示。这些患者常合并反复淋巴水肿(肢体肿胀加重)、皮肤增厚(象皮肿样改变)或乳糜性胸腹水(淋巴管瘘),却被传统三联征的框架忽略。
深静脉系统的“隐匿病变”:约30%-50%的KT患者存在深静脉发育不良(如股静脉缺如、髂静脉狭窄)或功能性梗阻(瓣膜功能不全),而非单纯的浅静脉扩张。这类患者若仅处理浅静脉曲张,可能因深静脉回流未改善导致症状复发甚至加重。
骨骼肌肉系统的“动态失衡”:肢体肥大不仅是软组织增生,更伴随骨骺过度刺激(患侧下肢骨生长速度比健侧快1.5-2倍),导致骨骼畸形(如胫骨弯曲、足弓塌陷)、关节负荷不均(膝踝关节炎发生率高达40%)及步态异常。
基因层面的“潜在调控异常”:近年研究发现,部分KT患者存在PIK3CA基因体细胞突变(约占30%-50%),该基因参与血管内皮生长因子(VEGF)信号通路调控,可能解释了血管/淋巴管异常增生的共同机制——但并非所有患者均携带该突变,提示KT可能是“多基因+环境因素”共同作用的结果。
这些发现彻底颠覆了“KT=单纯静脉畸形”的传统观念:它更可能是一种以血管/淋巴管发育异常为表型,涉及多系统(骨骼、皮肤、淋巴)及分子信号通路(PIK3CA等)调控失衡的复杂先天性系统性疾病。

二、诊断困境:当“典型表现”遇上“个体差异”
(一)临床分型的混乱与争议
目前国际上对KT综合征尚无统一的分型标准,常见的分类方式包括:
按血管异常主导类型分型:静脉型(以浅/深静脉发育异常为主)、淋巴-静脉型(合并淋巴管缺如)、动静脉瘘型(罕见,但可能导致严重高流量动静脉分流)。
按肢体受累范围分型:局限性(仅下肢局部受累)、弥漫性(整肢或双下肢受累)。
按并发症主导分型:以疼痛/肿胀为主、以肢体功能障碍为主、以皮肤溃疡/出血为主。
但这种分型在实际应用中问题重重:同一患者可能同时存在静脉扩张、淋巴管缺如和轻微动静脉瘘(影像学难以完全识别);“局限性”与“弥漫性”的界限模糊(病变可能随生长发育逐渐扩展);并发症的出现时间差异极大(有的儿童期仅表现为红斑和轻微肥大,成年后因深静脉血栓才出现严重症状)。
(二)诊断技术的“盲区”与互补需求
目前KT综合征的诊断依赖“临床三联征+影像学验证”,但每种技术均有其局限性:
超声检查:是首选的初筛工具,可显示浅静脉曲张、深静脉发育异常(如缺如、狭窄)及部分淋巴管扩张,但对深层结构(如骨骺生长板受刺激情况)及微小淋巴管缺如的分辨率不足;
MRI/MRA:能清晰显示软组织增生、骨骼长度差异及深静脉走行,但对淋巴管的直接成像仍依赖间接征象(如皮下组织增厚伴信号异常),且检查时间长、儿童配合度低。
淋巴造影:理论上可直观评估淋巴管通畅性,但因有创性(需注射造影剂至皮内淋巴管)和并发症风险(感染、过敏),临床极少常规开展。
基因检测:PIK3CA突变检测(通过皮肤活检或外周血)对部分患者有提示意义,但阴性结果不能排除KT综合征(约50%患者无该突变),且检测成本高、普及率低。
更棘手的是,许多基层医院因缺乏经验,常将KT综合征误诊为“单纯鲜红斑痣”(忽略肢体肥大)、“下肢静脉曲张”(忽略红斑和骨骼异常)或“淋巴水肿”(忽略血管畸形)。笔者曾接诊过一例12岁患儿,外院因“左小腿静脉曲张”行硬化剂治疗,术后出现皮肤溃疡——进一步检查才发现其自幼存在左下肢红斑和轻度肥大,实为KT综合征合并深静脉发育不良,硬化剂治疗反而加重了回流障碍。
三、治疗争议:从“对症治疗”到“系统管理”的艰难平衡
(一)核心矛盾:治疗目标的不统一
KT综合征的治疗目标究竟是什么?不同学科的医生存在显著分歧:
血管外科医生可能优先考虑“消除静脉曲张”(预防血栓或出血)。
骨科医生关注“矫正骨骼畸形”(改善步态和关节功能)。
皮肤科医生聚焦“红斑的美观问题”(激光治疗鲜红斑痣)。
患者家属则最关心“肢体不对称是否影响孩子心理”或“未来能否正常运动”。
这种目标的分散性导致治疗策略常陷入“头痛医头”的困境——例如,单纯硬化剂注射曲张静脉可能因深静脉回流未改善而复发;过早进行骨骼矫形手术可能因肢体持续生长导致畸形复发;激光治疗红斑虽能改善外观,但对肢体肥大或疼痛无任何帮助。
(二)具体治疗手段的争议与实践反思
1. 静脉异常的处理:从“盲目干预”到“功能评估优先”
传统观点认为,KT综合征的静脉曲张需早期干预(如硬化剂注射、手术剥脱),但近年研究发现:部分患者的浅静脉曲张是代偿性表现(因深静脉发育不良导致静脉血回流至浅静脉系统)——若盲目闭合浅静脉,可能反而加重深静脉负荷,导致肢体肿胀加剧。
目前的共识是:
先通过影像学(如静脉造影、MRV)明确深静脉功能状态,再决定是否处理浅静脉:
若深静脉通畅(如股静脉直径正常、血流速度达标),浅静脉曲张可考虑硬化剂或微创手术。
若深静脉缺如或严重狭窄,则需优先解决深静脉问题(如通过介入球囊扩张或搭桥手术)。再评估浅静脉处理必要性:
对于无症状的轻度静脉曲张(仅影响外观),可暂不干预,避免过度治疗。
2. 淋巴系统的“隐形干预”:被忽视的关键环节
约60%的KT患者存在淋巴回流障碍(尽管未表现出明显水肿),这类患者若仅处理静脉问题,肢体肿胀可能持续进展。但目前淋巴系统的治疗手段极为有限:
保守治疗:弹力袜/弹力绷带(压迫浅静脉和部分淋巴管)、淋巴引流按摩(需专业康复师指导)。
手术干预:如淋巴管-静脉吻合术(适用于淋巴管缺如但邻近静脉功能正常的患者),但因技术难度高、远期效果不确定,仅少数中心开展。
新兴探索:间充质干细胞注射(促进淋巴管再生)或基因靶向治疗(针对PIK3CA突变调控淋巴管发育),目前仍处于动物实验或小样本临床研究阶段。
临床实践中,我们常建议患者长期佩戴定制弹力袜(从儿童期开始),虽不能逆转淋巴管缺如,但能显著延缓肿胀进展——一位坚持佩戴10年的成年患者坦言:“如果不穿袜子,下午腿会比早上粗3cm,走路像灌了铅;但穿了袜子,至少能正常上班。”
3. 骨骼肌肉问题的“生长管理”:时机比手术更重要
肢体肥大伴随的骨骼过度生长是KT综合征最棘手的并发症之一。儿童期若不干预,可能导致双下肢长度差异超过5cm(严重影响行走),甚至继发脊柱侧弯。传统解决方案包括:
短缩健侧肢体(通过骨骺阻滞术限制健侧生长)。
延长患侧肢体(通过外固定支架牵拉骨骼,但手术创伤大、并发症多)。
观察等待(对于差异<2cm的患儿,通过鞋垫垫高平衡步态)。
但目前尚无绝对最优策略——短缩健侧可能影响整体身高发育;延长患侧需多次手术且存在感染/骨不连风险;而单纯观察可能导致患儿因步态异常产生心理问题。笔者的经验是:建立“骨骼生长监测档案”(每6个月测量双下肢长度、评估步态),在差异达到3cm前制定个性化方案(如差异2-3cm时优先定制矫形鞋垫,差异>3cm且年龄>8岁考虑骨骺阻滞术)。
4. 皮肤病变与并发症的“细节管理”:容易被低估的问题
鲜红斑痣在KT综合征患者中常伴随增厚或结节化(成年后发生率约20%),可能因摩擦导致出血或溃疡;浅静脉曲张严重者可能出现皮肤色素沉着、脂溢性皮炎甚至慢性溃疡。这类问题虽不致命,却显著影响生活质量——一位25岁的患者因小腿红斑结节反复破溃,最终发展为慢性骨髓炎,不得不接受局部皮瓣移植。
四、未来方向:从“经验性治疗”到“精准医学”的突破可能
(一)PIK3CA基因相关治疗的探索
约30%-50%的KT综合征患者携带体细胞PIK3CA突变(主要位于热点区域如E542K、E545K),该基因通过激活VEGF信号通路促进血管/淋巴管异常增生。针对这一靶点的靶向药物(如阿培利司,原用于乳腺癌PIK3CA突变治疗)已在国外开展小样本临床试验——初步结果显示,局部外用PIK3CA抑制剂可缩小部分患者的血管畸形范围,但全身用药的安全性(如高血糖、腹泻等副作用)仍需验证。
未来若能通过无创检测(如皮肤活检或液体活检)明确患者是否携带PIK3CA突变,并针对性应用靶向治疗,可能为KT综合征提供“对因干预”的新思路。
(二)患者教育与长期管理的科普缺失
许多KT综合征患者因“不致命”而被忽视——家长认为“胎记不用治”,患者觉得“腿粗点不影响生活”。但实际上,未规范管理的KT综合征可能导致成年后慢性疼痛、深静脉血栓甚至截肢风险增加。未来需加强基层医生的识别能力(如通过典型三联征早期筛查),并通过科普宣传让患者理解“早期干预”的意义(如儿童期佩戴弹力袜可延缓骨骼畸形)。
结语:KT综合征的诊疗启示——医学的复杂性在于“看见具体的患者”
KT综合征的百年认知史,本质上是一场从“局部表型”到“系统本质”的探索之旅。它提醒我们:临床医学中那些看似“典型”的疾病,往往隐藏着更复杂的真相——一条红斑下的静脉异常,可能牵连淋巴管、骨骼、基因甚至患者的心理健康;一套标准化的诊疗指南,永远无法覆盖每个患者的独特需求。
作为医生,我们或许无法立刻攻克KT综合征的所有难题,但至少可以做到:不再用“单纯血管畸形”的标签简化患者的痛苦,不再用“典型三联征”的框架限制诊断的视野,而是在每一次查房、每一次影像解读、每一次治疗决策中,看见那个具体的、有血有肉的患者——他可能只是希望腿不那么疼,能和同学一起跑操;她可能只想穿一条短裙,不用遮掩腿上的红斑。这,才是医学最本真的意义。
版权声明:
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理

