新三唑类药物—泊沙康唑,这些用法你都知道吗?
2021-09-02 03:30
阅读:27747
来源:医学用药参考
作者:医****考
责任编辑:医学用药参考
[导读] 泊沙康唑作为新一代三唑类抗真菌药物,与棘白菌素和其他三唑类药物相比,抗菌谱更广,抗菌活性较强,耐受性好,在侵袭性真菌病(IFD)的预防和治疗领域适用范围广泛。
泊沙康唑属于三唑类抗真菌药,由原先灵葆雅公司研发,2005年以口服混悬液制剂经美国食品药品监督管理局批准后上市。随后,又相继推出肠溶片、注射剂。目前经我国批准上市的只有泊沙康唑口服混悬液和肠溶片。泊沙康唑作为新一代三唑类抗真菌药物,抗菌谱既包含常见的念珠菌、隐球菌和曲霉,也包含毛霉、球孢子菌、镰刀菌、多育赛多孢子菌等罕见真菌。与棘白菌素和其他三唑类药物相比,泊沙康唑抗菌谱更广,抗菌活性较强,耐受性好,在侵袭性真菌病(IFD)的预防和治疗领域适用范围广泛。
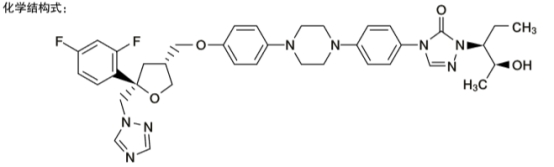
泊沙康唑通过化学结构改造,在三唑类母环基础上延伸出一条侧链,苯环中氟取代氯,同时侧链进行羟基化,使其和真菌亲和力更强,稳定性更高,细胞毒性增加,在保留药物亲脂性的同时水溶性增加,更容易进入组织并释放。另外,长侧链结构增加了药物对靶点(CYP51)的亲和力,对CYP450酶影响更小,仅是CYP3A4抑制剂,药物活性更高、更安全,而且受14α-脱甲基酶密码子突变的影响更小,与跨膜转运蛋白(外排泵)的结合力更低,更不容易耐药。其化学名称及化学结构如下:
化学名称:4-[4-[4-[4-[[(3R,5R)-5-(2,4-二氟苯基)四氟化-5-(1H-1,2,4-三唑-1-甲基)-3-呋喃]甲氧基]苯基]-1-哌嗪基]苯基]-2-[(1S,2S)-1-乙基-2-羟丙基]-2,4-二氢-3H-1,2,4-三唑-3-酮
泊沙康唑与其他三唑类抗真菌药物作用机制相似,主要通过抑制CYP450依赖的14α-脱甲基酶进而抑制麦角甾醇的合成,导致真菌细胞膜的生物合成障碍,细胞膜通透性改变,从而抑制真菌生长。泊沙康唑主要在胃部溶解,在十二指肠部位吸收。剂型不同,泊沙康唑的吸收也会有差异。混悬液口服后3h达血药峰浓度(Cmax),7~10d达稳态血药浓度。泊沙康唑肠溶片口服后达峰时间为4~5h,其包衣由pH值敏感聚合物稳定剂赋形剂组成,可限制泊沙康唑在胃中的低pH值释放,并在小肠的中性pH值释放泊沙康唑,可显著提高药物吸收,空腹条件下,泊沙康唑肠溶片与混悬剂相比,生物利用度提高了3倍。而泊沙康唑注射剂无吸收过程,几乎在注射完毕时即可达血药峰浓度,适用于不能耐受口服剂型的患者。既往研究表明泊沙康唑混悬液与食物同服后,其药时曲线下面积(AUC)和峰浓度(Cmax)比空腹给药增高近3~4倍,而泊沙康唑肠溶片主要在肠道释放并吸收,故其体内吸收受食物影响较小。泊沙康唑混悬液的吸收随胃液pH值的升高或胃肠蠕动的增加而降低。而泊沙康唑肠溶片体内吸收几乎不受胃液pH值与胃肠道蠕动影响。泊沙康唑血浆蛋白结合率高达98%,具有良好的组织渗透性,表观分布容积1774L,可广泛分布于全身。该药可经过肝脏二磷酸尿苷葡萄糖苷酶(UDP-葡糖苷酶)系统代谢为无生物活性的代谢产物,后经肠道P糖蛋白-ATP依赖的细胞膜转运蛋白,从细胞内排出。泊沙康唑半衰期约为35h,规律使用6~7d后达稳态浓度,77%泊沙康唑主要以原型药物经粪便排泄,其余以代谢产物经肾排泄。血液系统疾病患者本身多存在白细胞质量及数目的异常,当接受化疗,尤其是高强度化疗后,自身免疫功能进一步降低,极易发生IFD,临床上推荐应用泊沙康唑、伊曲康唑等进行预防给药。对急性髓细胞白血病/骨髓增生异常综合征(AML/MDS)(中性粒细胞减少)患者,泊沙康唑是国内外权威指南高级别推荐的抗真菌预防药物,其中明确指出,急性白血病(包括MDS)初次诱导或挽救化疗患者、预期粒细胞缺乏持续>10d、伴有严重粒细胞缺乏等高危因素的患者应进行预防治疗,药物首选泊沙康唑,其次为氟康唑、伊曲康唑及伏立康唑等.2018年西班牙的一项真实世界研究显示,在接受强化化疗的AML/MDS患者中,泊沙康唑预防治疗组后续经验性治疗及治疗失败率显著低于伊曲康唑组。计建军等泊沙康唑预防侵袭性真菌感染疗效及安全性的Meta分析结果表明,泊沙康唑预防疗效优于氟康唑(P<0.0001)和伊曲康唑(P=0.001),证实或很可能是侵袭性真菌感染引起的死亡率泊沙康唑均低于其他抗真菌药,且未增加不良反应的发生率。(二)、预防造血干细胞移植(HSCT)患者发生IFD异基因造血干细胞移植(allo-HSCT)是发生IFD的高危因素,接受allo-HSCT的恶性血液病患者无论是在预处理后的粒细胞缺乏期还是在使用免疫抑制剂治疗移植后排异反应期间都容易发生IFD,对此类患者进行预防性抗真菌治疗是十分必要的。现有的相关循证医学证据支持将泊沙康唑做为allo-HSCT预防性抗真菌治疗的首选药物。预防应从预处理开始,疗程覆盖整个粒细胞缺乏期,HSCT治疗患者一般至少覆盖移植后3个月,伴移植物抗宿主排异反应的患者预防应持续至反应消失或免疫抑制剂停用。治疗口咽念珠菌病是泊沙康唑的重要适应证之一,对于氟康唑或伊曲康唑等治疗失败的难治性口咽念珠菌病,泊沙康唑可作为首选治疗药物。一项针对人类免疫缺陷病毒感染者继发口咽念珠菌病或食道念珠菌病的国际多中心、Ⅲ期、开放性临床研究显示,对于氟康唑和/或伊曲康唑治疗失败的患者,泊沙康唑治疗28d临床应答率高达75%,因不良反应终止治疗的比例仅4%。对于存在毛霉感染流行环境暴露的粒细胞缺乏患者患者,建议将泊沙康唑作为预防性抗真菌治疗的首选药物。在毛霉病的初始治疗中,建议泊沙康唑作为两性霉素B类抗真菌药物的备选,用于病情稳定的非危重患者或不能使用两性霉素B类抗真菌药物的患者。在毛霉病的挽救性治疗中(包括难治性病例及不能耐受病例),泊沙康唑可作为替换两性霉素B类抗真菌药物的首选药物。泊沙康唑作为强效的CYP3A4抑制剂,会导致经CYP3A4代谢的其他药物血药浓度升高,但是对CYP450酶系统中其他亚型的活性没有影响。1.西罗莫司:口服泊沙康唑重复剂量给药,西罗莫司的Cmax和AUC分别平均增加6.7倍和8.9倍。当服用西罗莫司的患者开始泊沙康唑治疗时,应该减少西罗莫司的剂量(例如:减少至当前剂量的1/10),并频繁监测西罗莫司全血谷浓度。开始给药之前、同时服用期间和泊沙康唑治疗终止时应进行西罗莫司浓度监測,并相应地调整西罗莫司剂量。2.他克莫司:泊沙康唑可导致他克莫司的Cmax和AUC值分别显著增加121%和358%。在开始泊沙康唑治疗时,将他克莫司的剂量减至初始剂量的约三分之一。在泊沙康唑治疗期间和停止治疗后应该频繁监测他克莫司的全血浓度谷值,并且依据此调整他克莫司的剂量。3.环孢菌素:在开始泊沙康唑治疗后,泊沙康唑口服混悬液200mg每日1次可导致心脏移植患者的环孢菌素全血浓度升高。建议在开始泊沙康唑治疗时,将环孢菌素的剂量减至初始剂量的约四分之三。在泊沙康唑治疗期间和停止治疗后应该频繁监测环孢菌素的全血浓度谷值,并且依据此调整环孢菌索的剂量。泊沙康唑与CYP3A4底物,如匹莫齐特和奎尼丁联合用药可导致上述药品的血浆浓度升高,从而导致QTc间期延长和罕见的尖端扭转型室性心动过速。因此,禁止泊沙康唑与这些药物联用。(三)、通过CYP3A4代谢的HMG-CoA还原酶抑制剂(他汀类药物)口服泊沙康唑重复剂量给药,辛伐他汀的Cmax和和AUC平均分别增加7.4至11.4倍和5.7至10.6倍。增加血浆中HMG-CoA还原酶抑制剂浓度可能伴随横纹肌溶解症。因此禁止泊沙康唑与主要通过CYP3M代谢的HMG-CoA还原酶抑制剂同时服用。大多数麦角生物碱都是CYP3A4底物。泊沙康唑会导致麦角生物碱(麦角胺和双氧麦角胺)血浆浓度升高,可能导致麦角中毒。因此,禁止泊沙康唑与麦角生物碱联用。泊沙康唑与咪达唑仑联合用药会导致咪达唑仑血浆浓度约升高5倍。另外,同时服用期间口服泊沙康唑可导致咪达唑仑的平均终末半袞期从约3-4小时延长至8-10小时。而咪达唑仑血浆浓度升高则会增强并且延长催眠和镇静作用。泊沙康唑与其他通过CYP3A4代谢的苯二氮卓类药物(例如,阿普唑仑、三唑仑)联合用药也会导致这些苯二氮卓类药物血浆浓度升高。因此必须密切监测治疗患者是否发生由于通过CYP3A4代谢的苯二氮卓类药物血浆浓度过高导致的不良反应,并且必须备有苯二氮卓受体拮抗剂用于逆转这些反应。与泊沙康唑同时服用期间建议考虑调整通过CYP3A4代谢的苯二氮卓类药物的剂量。[1]刘洁,胡小平,刘伟.三唑类抗真菌新药泊沙康唑和伏立康唑简介[J].菌物学报,2018,37(10):1391-1398.[2]泊沙康唑临床应用专家组.泊沙康唑临床应用专家共识[J].国际呼吸杂志,2020,40(4):241-261.[3]叶珍洁,吴灵洁,张晓颖,郑玲.泊沙康唑药动学及其治疗药物监测方法研究进展[J].药物评价研究,2021,44(01):222-228.[4]计建军,张慧,查丽,等.泊沙康唑预防侵袭性真菌感染疗效及安全性的Meta分析[J].实用药物与临床,2021,24(3):229-236.[5]张飞雨,张瑞霞,宋学武,张弋.影响泊沙康唑血药浓度相关因素的研究进展[J].中国医院药学杂志,2021,41(09):971-976.[6]泊沙康唑口服混悬液说明书.2019年版.英国默沙东MerckSharp&DohmeLtd.