ITX5061新药具有一定的抗丙肝病毒作用
2013年10月9日发表在《JInfectDis》上的一项研究旨在评估ITX5061治疗HCV患者的有效性和安全性,并且初步确定最佳用药方案。HCV进入细胞涉及到清道夫受体B1(SR-B1)。在体外,ITX5061抑制SR-B1能够阻止HCV的复制。
研究设计
研究者在未治疗的、无肝硬化的、感染HCV基因型1型的患者中进行了多中心研究来评估ITX5061的安全性和抗病毒活性。基于先前设定的安全性和活性标准(8人中有不少于4人的HCVRNA下降≥1log10IU/ml,研究者设计了随着治疗间期的延长(3,14,28天)或剂量递减(150,75,25)的连续群组,群组以10人为一个群体(ITX5061治疗8人,安慰剂2人)。
研究结果
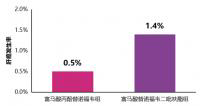
三组共有30人:每日口服ITX5061150mg持续时间分别是3天(A150)、14天(B150)和28天(C150)。6人有等级大于等于3的不良反应(安慰剂组中有1人);但都与治疗无关。在7名C150组人中,有1人(14.3%,95%CI0.7%-55.4%)的HCVRNA(1.49log10IU/mL)下降幅度大于等于1log10IU/mL,而在其他6人安慰剂组、8人A150组或8人B150组中都没有类似的下降。
结论
总之,每日口服ITX5061150mg维持28天是安全的,耐受良好的。在28天组中,7人中有1人显示有抗病毒活性;然而,先前设定的抗病毒活性的标准在剂量和持续时间研究中都没有达到。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]