《Genes&Development》:终末期肝病的关键性发现
目前,亚利桑那大学(UA)药学院的一个研究小组,发现了一个未知的分子通路,对于开发减缓甚至扭转终末期肝病进展的新疗法非常关键。
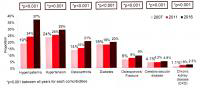
虽然肝硬化一般都与酒精或药物滥用有关,这种疾病——特点是瘢痕组织替代正常肝组织,也可能起因于病毒性肝炎、肥胖和糖尿病以及某些遗传性疾病。根据美国**卫生研究院资料显示,肝硬化是美国第12大疾病死亡原因。正如许多其他人类病理情况一样,终末期肝病与氧化应激密切相关,氧化应激指的是,通过活性氧分子损伤使生物组织遭受损伤。这些分子,也被称为自由基,作为体内代谢过程的副产品自然发生,与许多慢性疾病有关,包括癌症、糖尿病、神经退行性疾病和心血管疾病。
UA药理学和毒理学系教授Donna Zhang称:“细胞通过各种机制,控制氧化应激。”她解释说,这些机制大部分都包括Nrf2——几乎存在于每个细胞的一个蛋白,起分子开关的作用。Nrf2可激活细胞内不同的生化机制,捕捉活性氧分子,或在受损细胞组分造成更多的麻烦之前处理它们。许多水果和蔬菜中发现的抗氧化剂,通过捕捉活性氧分子而发挥它们对健康的益处。
在正常健康的状况下,当不需要应激反应时,一种称为Keap1的酶,会不断消耗Nrf2,保持其较低水平。
Zhang解释说:“那么,在来自活性氧分子的压力下,或当你从某些植物(如西兰花豆芽)中摄取抗氧化剂时,它会阻止Keap1消耗Nrf2,使其在细胞内积累。然后,Nrf2会激活细胞的抗氧化反应。这就是抗氧化剂如何发挥作用。”根据传统观点,我们身体在受到高氧化应激时,会打开它们的Nrf2介导的保护途径,来限制来自破坏性含氧化合物的损伤。在肝硬化阶段,Nrf2应该由氧化应激诱导,但是到这项研究为止,由于不明原因,这种情况没有发生。
Zhang说:“这是我们开展这项研究之前所遇到的一个难题。不知何故,Nrf2介导的保护机制被另一个因素损害,而不是肝硬化中的Keap1。”另外,旨在抑制Keap1消耗Nrf2的药物在肝硬化中已被证明无效。
当Zhang和她的同事们研究了取自肝硬化患者的肝组织样本时,他们发现了面对猖獗的氧化应激时令人费解的Nrf2低水平其背后的原因。
原来,另一种酶会消耗Nrf2并阻止急需的抗氧化反应,加剧了疾病的进程。蛋白质Hrd1是细胞垃圾处理的部分——在错误折叠蛋白质积累和破坏细胞成分之前,专门破坏它们。
Zhang解释说,在正常情况下,Hrd1水平很低,所以它不会过多干扰Nrf2。随着肝硬化的进展,过度的炎症会触发垃圾介导的应激反应,并且Hrd1变得非常丰富,开始消耗Nrf2。
相关研究结果发表在2014年4月刊的《Genes and Development》杂志。第一作者是UA药理学和毒理学系的研究生Tongde Wu,这是其毕业论文的一部分。同一部门的Fei Zhao和Eli Chapman也参与了这项研究。这项工作开始于Zhang和西北大学费因伯格医学院Deyu Fang、Beixue Gao和Can Tan研究小组的合作。其他参与者还包括日本圣玛莉安娜大学的Naoko Yagishita和Toshihiro Nakajima和UA工程学院的Pak K. Wong。
这一发现可能改变科学家开发疗法的方式,因为它为未来药物提供了一个新靶点。在实验室实验中,Zhang和她的同事们能够通过灭活Hrd1恢复肝硬化中的Nrf2水平,有效地逆转小鼠的肝硬化。
Zhang说:“以前的工作主要集中在Keap1蛋白,并试图阻止其对Nrf2的破坏。现在我们知道了其中的第二个因素——Hrd1,为了恢复Nrf2的水平,我们需要抑制它。”
她强调说:“促进Nrf2有利于一般的保护,这就是为什么你应该经常吃西兰花的原因。”
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]