【FDA】首个治疗罕见胆汁酸合成障碍新药获FDA批准
FDA的一份新闻稿显示,FDA批准Cholbam,一种胆酸,用于胆汁酸合成障碍和过氧化物酶体紊乱的儿童和成人。
药商获批罕见儿科疾病优先审查后,FDA宣布批准Cholbam(胆酸,Asklepion制药有限责任公司)用于成人和3岁以上儿童口服治疗。新闻稿中称,胆汁酸合成障碍和过氧化物酶体紊乱患者缺乏合成胆酸(肝脏分解胆固醇所生成的一种原胆酸)所需的酶,如果不治疗,可能出现威胁生命的肝损伤。
“FDA审批Cholbam对胆汁酸缺乏性疾病患者和家庭来说至关重要,” 旧金山加州大学小儿肝病主任,Philip Rosenthal博士在一份新闻稿中说。“以前,依赖这种救命药的患者只能通过研究试验来获取药物。这种罕见疾病科学和协作的显著成就使这一疗法更广泛的应用。”
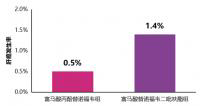
在确定胆酸疗效的临床试验获得成功后,Cholbam通过审批。50例患者进行了18年以上的胆汁酸合成障碍治疗。治疗后,基线肝功能检测及体重明显改善。治疗结束后,一半以上的患者存活3年以上。对于过氧化物酶体疾病的治疗,29例患者进行了18年以上的治疗。多数患者开始治疗时在2岁以下(3周-10岁)。治疗后,这一患者人群的基线肝功能检测和体重可见改善,42%的患者存活3年以上,新闻稿显示。治疗患者最常见的不良事件是腹泻。
“这个批准强调了机构为缓减疾病患者提供治疗的承诺,” FDA药品评价和研究中心药物评价III所的办公室主任Julie Beitz博士在新闻稿中称。“批准之前,胆汁酸合成障碍患者没有获批的治疗方案。”
FDA建议有经验的肝病或小儿胃肠病专家全面监测这种治疗方法,肝功能恶化患者应终止治疗,新闻稿中称。
编译自:FDA approves first treatment for rare disorders in children, **s. Healio, 2015.
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]