诺贝尔得主详细解剖神经递质释放过程
今年荣获诺贝尔生理学或医学奖的三位科学家就是在这个细胞基本过程中作出了杰出贡献,他们的发现对于我们理解“货物”如何在正确的时间、在细胞内外被精确地输送具有非常重要的影响。从酵母到人,不同的生物体利用相同的机制进行囊泡的输送和融合。
其中来自斯坦福大学的ThomasC.Südhof教授主要贡献在于阐释了信号如何指导囊泡精准地释放其“货物”的原理,近期他在《NatureMedicine》杂志上发表文章,详细介绍了神经递质释放过程的分子机制。
囊泡通过同神经细胞的外膜结合,从而将信号分子神经递质释放出来但是,这些囊泡只有在神经细胞需要给临近的神经细胞发送信号时,才被允许将其包含的神经递质释放出来。那么,如何对这种释放进行精确地控制呢?
科学家们此前已经知道,钙离子与这一过程有关。在上世纪90年代,Südhof就开始在神经细胞中搜寻钙离子敏感蛋白。最终,他阐明了对大量钙离子进行应答并指导临近的蛋白快速地让囊泡同神经细胞的外层膜相结合的分子机制—拉链被打开,信号物质释放出来。他的发现解释了如何获得这种时间上的精确性以及囊泡内的“货物”如何被按需释放。
Südhof表示,他的研究成果与其它研究共同揭示了一个合理机制——解释了膜在递质释放过程中如何快速融合,这些融合又是如何受到钙离子的调控,以及突触囊泡钙离子调控融合是如何在突触前终端进行快速组织的。
然而,随着许多研究成果的公布,也出现了更多新的问题,这些问题十分重要,比如说融合的精确物理化学机制,在大脑疾病病理过程中,融合机制扮演了什么样的角色?这一领域还有许多工作有待科学家们探索。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
细数20年间卒中二级预防进展历程
让我们首先从抗血小板疗法来进行讨论。毫无疑问的是,阿司匹林对于卒中的二级预...[详细]
-
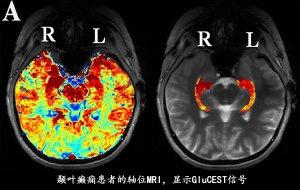
新型MRI成像技术可有效检出癫痫病灶
研究者正在尝试使用一种有力的影像学检查工具,对难以寻觅的癫痫病灶进行定位。...[详细]