FDA更新丙肝药Olysio标签
FDA最近宣布对Olysio的产品标签进行了修订,Olysio是用于与利巴韦林和聚乙二醇干扰素联合治疗丙型病毒性肝炎成年患者。
Olysio(司美匹韦,Janssen Therapeutics)的标签修订包括对HCV基因型1和4感染患者服用剂量和治疗持续时间,以及治疗HCV/HIV合并感染信息的更新。更新包括:
初治患者和先前有过复发的患者,无HIV感染的伴或不伴肝硬化的患者、合并感染HIV的不伴肝硬化的患者,应该采用司美匹韦联合PEG-IFN-a和利巴韦林治疗12周,随后PEG-IFN-a和利巴韦林再补充治疗12周的方案。
先前有过复发的HCV/HIV合并感染有肝硬化的初治患者,应该采用司美匹韦联合PEG-IFN和利巴韦林治疗12周,随后PEG-IFN和利巴韦林治疗36周的方案。
之前治疗无应答的患者,不管是否伴有肝硬化,是否为HCV/HIV合并感染,都建议其采用司美匹韦联合PEG-IFN和利巴韦林治疗12周,随后PEG-IFN和利巴韦林治疗36周的方案。
此次修订是由临床数据所支持的,根据公告,在106例HCV基因型1/HCV合并感染患者以及107例HCV基因型4感染患者中,司美匹韦联合PEG-IFN和利巴韦林治疗有很好的安全性。两组患者用药的安全性与HCV基因型1单一感染患者是相似的。
Olysio产品标签修订的其他内容包括:
药代动力学方面包括了HCV/HIV合并感染患者的信息;
] 微生物学方面包括了HCV基因型4的数据;
临床研究反映了HCV/HIV合并感染以及HCV基因型4试验的结果。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
- 相关阅读
- ·黄热病的鉴别诊断
- ·执业医师考试病理学速记
- ·乙肝面前,医务人员如何做好职业防护?
- ·病毒性肝炎疾病预防
- ·黄疸型肝炎的诊断措施
热点图文
-
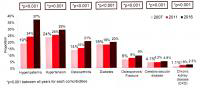
AASLD2018研究进展丨慢乙肝患者治疗期间的肾脏安全管理
在新药取得成功之前,应用口服核苷(酸)类似物(NA)治疗慢性乙型肝炎(简称...[详细]
-
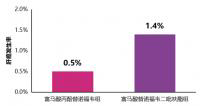
快讯丨TAF治疗4年的肝细胞癌发生率低于TDF
5月17日,在第十届全国疑难及重症肝病大会上,我国香港大学司徒伟基教授交流...[详细]