肺癌患者脑部寡转移,肺部肿瘤经手术切除治疗获得长期生存
病例资料
患者,女,70岁,因“体检发现肺部肿物20多天”于2022-05-30入院。患者20多天前于当地医院体检时,查胸部CT发现右肺上叶肿物。入院后,完善相关检查。2022-05-31颅脑MRI示:两侧半卵圆中心多发缺血灶。左侧枕叶细小强化结节,考虑转移。2019-06-01胸部+上腹部增强CT示:右肺上叶后段占位灶,最大径为2.7cmx2.8cm,有分叶及毛刺征,首先考虑周围型肺癌。2022-06-10 CT引导下穿刺病理示:(右肺肿块穿刺)腺癌。基因检测示:EGFR Ex19缺失突变。未见ALK/ROS1突变。支气管镜、肿瘤标志物、全身骨显像、心超、肺功能均未见明显异常。
初步诊断:右肺上叶腺癌,周围型,脑转移,cTlcNOM1b,IIVA期(AJCC第八版,2017),EGFR Ex19缺失突变。
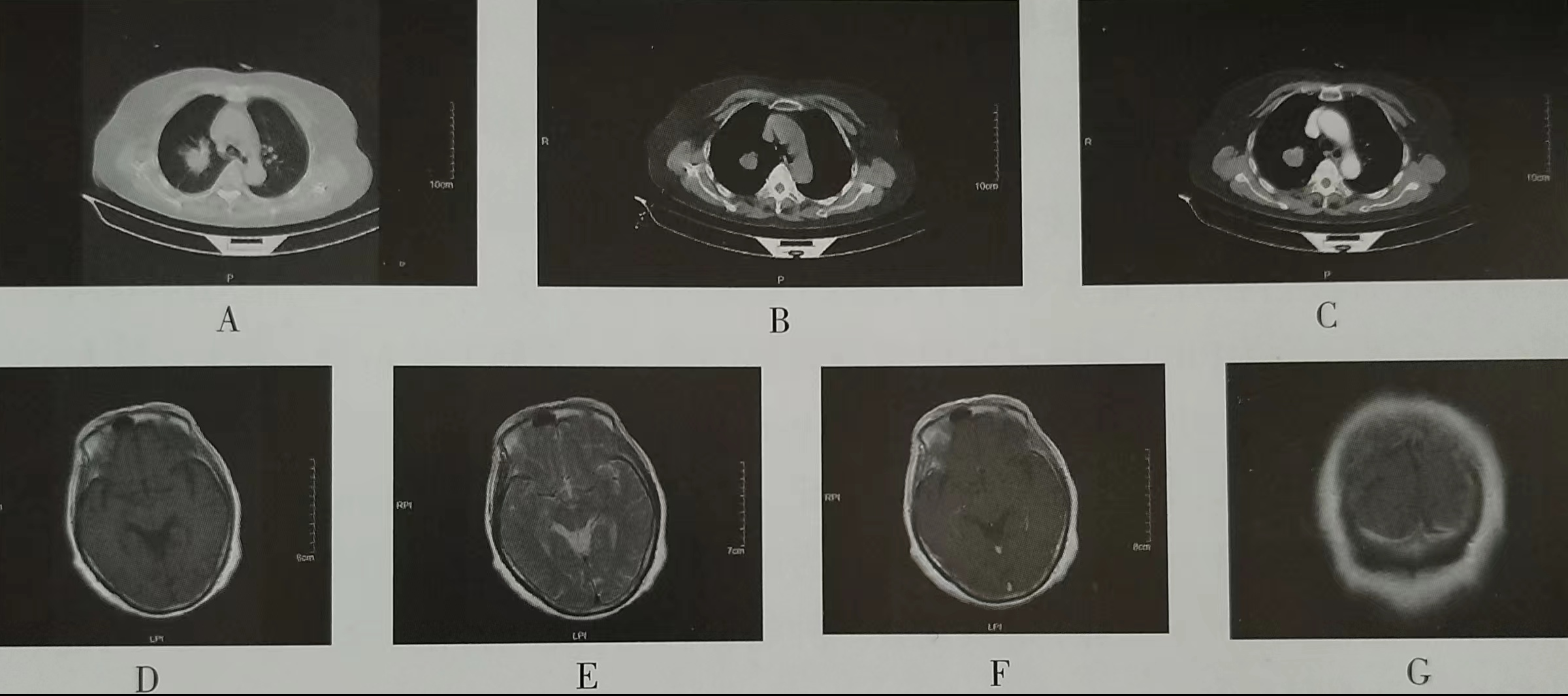
图1为胸部增强CT、颅脑增强MRI:右肺上叶后段周围型肺癌(A~C),伴左侧枕叶结节,考虑转移(D~G)。
第一次MDT组讨论与治疗情况
讨论情况
影像科:右肺上叶后段占位灶,最大径为2.7cmx2.8cm,有分叶及毛刺征,边界尚清晰,增强后病灶内有较明显的不均性气候,首先考虑周围型肺癌;左侧枕叶细小强化结节,结合病史,考虑转移的可能性大。影像分期:T1N0M1。
病理科:本例穿刺病理显示纤维组织内有少量的条索状、腺管状癌组织,形态符合腺癌。
胸外科:目前诊断考虑为右上肺腺癌,伴脑部转移,分期为IVA期,属于晚期,暂无手术指征,应首先考虑全身治疗。
肿瘤内科:晚期肺腺癌,无症状脑孤立转移,驱动基因EGFR敏感突变,在治疗的选择上国内外指南均推荐一线使用EGFR-TKI靶向治疗,一、二、三代EGFR-TKI都是I类证据推荐,但是三代奥希替尼是优先推荐的,特别是对于脑转移的患者。据研究,第一代/第二代EGFR-TKI的脑脊液穿透率最多为5%。相比之下,APOLLO研究的结果显示,奥希替尼的脑脊液穿透率为31.7%。在III期FLAURA试验中,将奥希替尼与一代靶向药(吉非替尼、厄洛替尼)作比较用于一线治疗EGFR Ex19缺失和Ex21 L858R突变的患者。对于CNS转移的患者,奥希替尼组的中位PFS明显延长,分别为15.2m vs 9.6m。
放疗科:患者有EGFR敏感突变脑转移肺腺癌,EGFR突变型肺癌较EGFR野生型容易出现颅内转移,风险高3~5倍左右。因此,目前,EGFR敏感突变或ALK-EML4融合阳性被认为是非小细胞肺癌患者脑转移发生风险增加的重要因素;目前虽然有脑转移,但是暂时没有脑转移引起的临床症状,比如头晕、头痛、呕吐等,建议给予入脑浓度高的EGFR三代TKI药物进行治疗,观察脑转移临床症状变化,治疗过程中若有不良症状新发,则尽早进行放疗。GPA(the Graded Prognostic Assessment)脑转移性肿瘤预后评估系统是目前最优的评价脑转移患者预后的预测工具。分子靶向药物被广泛使用后,基于分子标记的GPA系统(DS-GPA)也逐渐盛行。该患者的DS-GPA评分为3分,属于预后相对较好的肺癌脑转移患者,根据以往的回顾性试验研究数据,其中位生存时间为26.5个月。
讨论意见
经过团队的讨论,建议患者接受EGFR-TKI治疗,首先选择奥希替尼。
治疗情况
患者于2022-06-19起接受奥希替尼80mg QD治疗。2022-07-16复查胸部CT提示:右肺上叶后段占位灶,最大径为1.7cmx1.4cm,有分叶及毛刺征,较前2022-06-01CT缩小。疗效评价为PR。2022-12-12复查胸部CT提示:右肺上叶后段占位灶,最大径为1.7cmx0.6cm,有分叶及毛刺征,较前2022-07-16 CT缩小。疗效评价为PR。2023-03-17复查胸部CT提示:右肺上叶后段占位灶,最大径为1.7cmx0.6cm,有分叶及毛刺征,较前2022-12-12 CT大致相仿。疗效评价为PR。2023-03-17复查颅脑MRI:原左侧枕叶小结节状强化,此次不明显,建议复查。肿瘤标志物、支气管镜、全身骨显像、心超、肺功能均未见明显异常。
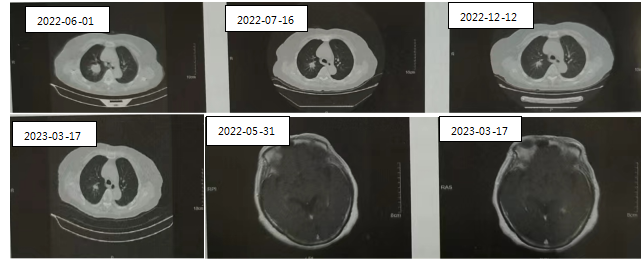
图2 右肺癌靶向治疗后多次随访复查右肺上叶后段病灶持续缩小,左侧枕叶转移瘤基本消退。
第二次MDT讨论与治疗情况
讨论情况
影像科:肺癌靶向治疗随访复查,多次肺部CT均显示作为靶病灶(非淋巴结病灶长径>1.0cm)的右肺上叶后段肺癌病灶较前持续缩小且长径缩小>30%,靶病灶疗效评价为持续PR。作为非靶病灶(未达到靶病灶条件)的右肺门淋巴结以及左侧枕叶转移瘤,目前已均基本消退,非靶病灶疗效评价为CR。根据RECIST1.1标准,此患者的整体疗效评价为PR。
胸外科:经过三代靶向药物治疗,患者取得了令人满意的疾病控制效果。右上肺病灶缩小明显,颅内病灶基本消失。在全身治疗取得良好疗效的情况下,可考虑加用局部治疗,进一步改善患者的疾病状况;同时,最近的复查结果提示肺部病灶相较前片未再见缩小,提示残余部分病灶对三代靶向药物的敏感性已不高。在这种情况下,建议对肺部病灶进行局部治疗以提高疾病控制率。对于晚期患者,放疗一般作为局部治疗的首选。但是,该患者不同于一般的晚期患者。首先,患者初始时就处于寡转移状态,仅有1枚脑部转移病灶,肺部原发病灶分期为T1N0;在接受全身治疗之后,不仅肺部原发病灶明显缩小,而且脑部转移病灶在MRI图像上已基本消失,均提示疾病控制良好。根据一项多中心回顾性研究的结果,同时接受了肺部原发病灶切除及脑部转移病灶切除的患者术后1年生存率为56%,2年生存率为28%,5年生存率为11%;提示预后良好的因素为肺部肿瘤直径小、无淋巴结转移、行完整肺叶切除、病理类型为腺癌。ACCP指南也认为在寡转移状态下的NSCLC合并脑转移的患者中,对于N分期为0~1且全身无其他转移病灶、肺部原发病灶可被彻底切除的患者,手术治疗对生存期有一定的获益。另外也有文献提示,年龄较小、KPS评分高、除了颅内转移外无其他部位转移,原发病灶控制良好的脑寡转移癌NSCLC患者,积极接受原发病灶的手术治疗是有益的。该患者符合所有的预后良好因素,预计能够从根治性肺叶切除手术中获益。在这一情况下,考虑到患者的一般情况尚可,心肺功能可耐受,颅内病灶影像学已完全消失,肺部病灶除放疗外亦可考虑采用根治性手术的方式,彻底切除右上肺叶病灶。手术方式可选择全麻胸腔镜下右肺上叶切除术+肺门纵隔淋巴结清扫术。
肿瘤内科:患者的奥希替尼的治疗效果佳,特别是脑部孤立病灶在影像学上已经消失了。对于肺癌寡转移的治疗,局部治疗很重要。考虑这例患者的特点是原发病灶小,原发疾病分期早,转移病灶也是孤立的,目前的转移病灶影像消失,建议原发病灶加局部治疗。
放疗科:对于EGFR敏感突变的晚期肺癌患者,EGFR-TKI的全身治疗是最主要的,但是药物治疗总有一天会出现耐药进展。因此,可以对TKI治疗期间出现进展的患者进行局部放疗,放疗也可以作为EGFR-TKI治疗的辅助手段。该患者目前处于后者阶段,即用于TKI治疗后尚未发生疾病进展但又未能获得完全缓解。但是,目前对于TKI使用中放疗何时介入的问题还没有定论。回顾性试验告诉我们,一般接受EGFR-TKI治疗的患者在药物治疗3个月后退缩达到最高峰。因此,较为理想的时间节点是TKI治疗后3个月。在2018年世界肺癌大会上,有一项来自我国上海胸科医院的一项回顾性临床研究,253例EGFR敏感突变的寡转移性非小细胞肺癌患者中有149例患者在接受EGFR-TKI治疗的同时联合局部巩固治疗;另外104例患者仅接受EGFR-TKI单独治疗。结果发现对EGFR敏感突变的寡转移性非小细胞肺癌患者,在EGFR-TKI治疗的基础上联合应用局部巩固治疗与单纯EGFR-TKI治疗相比,可使疾病进展或死亡风险降低43%,中位无进展生存时间分别为14个月和9个月;同时,局部巩固治疗使患者的总体死亡风险降低了44%,中位总生存时间分别为33个月和20个月;而且局部巩固治疗所带来的生存获益与EGFR突变亚型(EGFR Ex19缺失或Ex21 L858R突变)及转移部位均无关。因此,该患者可考虑加用放疗来控制肺部原发病灶。
讨论意见
经过团队的讨论,建议患者接受局部治疗。放疗与手术治疗均可。与患者商议之后,患者决定接受手术治疗,切除肺部原发病灶。
治疗情况
患者于2023-04-13行胸腔镜下右肺上叶切除术+肺门纵隔淋巴结清扫术。右上肺癌脑转移靶向治疗后术后常规病理示:①(右上)肺结节型(瘤体直径约为1.7cm)浸润性腺癌(腺泡为主型,局灶贴壁及乳头状生长,中分化),局灶见中分化鳞状细胞癌成分(所占比例<5%),侵及肺内支气管软骨,累犯大血管壁伴脉管瘤栓形成,癌周纤维组织增生、胶原化伴炎症细胞浸润(符合靶向治疗后改变)。②(第2/4组)4只、(第7组)6只、(第10组)5只、(第11组)4只、(第12组)2只淋巴结慢性炎伴结内炭末沉着。术后诊断:右肺上叶腺癌(部分鳞癌),脑孤立转移,ypT1bN0M1b,IVA期,EGFREx19缺失突变。患者术后继续服用奥希替尼80mgQD治疗,并定期复查。2023年8月及2024年1月复查胸部CT及颅脑MR,病情稳定,未见肿瘤进展。
总结
该病例的主要亮点在于该患者在服用三代靶向药,肺部原发病灶及脑内寡转移病灶均获得了良好控制的情况下,经过MDT讨论后,对肺部原发病灶进行了根治性手术切除。伴寡转移的NSCLC患者,何时适合接受外科干预,一直是讨论的热点。目前的NCCN指南中仅提到了在经过了全身治疗且疾病得到良好控制的情况下,对寡转移病灶进行局部治疗能够使患者获益,但未明确指出对原发病灶该如何处理。目前,针对寡转移病灶手术切除的研究较多,而在同一情况下涉及原发病灶手术切除的文献报道明显更少。
脑部是NSCLC患者最常见的远处转移部位,约20%的患者在病程中会出现脑转移。相对于其余部位,脑转移的NSCLC患者的预后总体较差,因此,外科介入需要更为慎重;仅对于部分预后较好的脑转移患者,手术切除可能使患者获益。目前,已有的文献均认为,若患者的肺部及区域淋巴结分期较早(T1~2N0),颅脑转移病灶的数量少且受到药物的良好控制,全身无其余转移病灶,一般情况良好,那么对肺部手术进行根治性切除是合适的。该患者的分期为T1N0M1,仅有1枚脑内转移病灶,而且在服用三代靶向药物后,肺部原发病灶及脑内转移病灶均得到了良好的控制。在脑转移患者中此类患者属于预后较好的,因此,值得进行肺部原发病灶根治性切除。
目前,有关脑部寡转移病灶患者的肺部原发病灶处理的研究仍然不足,已有的文献多为一些小样本回顾性研究的结果,缺少证据等级高的研究。此病例在已有文献的基础上进行了探索,施行了胸腔镜下肺叶切除术及肺门纵隔淋巴结清扫。根据随访结果,患者至截稿时未有疾病复发,仍处于良好控制的状态,证明这一探索的阶段性成功,希望能够为将来再次面对这类患者提供经验。但是,该患者的颅内病灶处于不可见的状态,并不意味着患者的脑内病灶得到完全缓解,而且脑内病灶未进行局部治疗,仍存在耐药、复发的风险。因此,该患者仍需密切关注脑内病灶及全身其余部位的复发情况,及时进行处理。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们
联系zlzs@120.net,我们将立即进行删除处理
热点图文
-
多参数MRI在前列腺癌精准诊断应用思考
随着前列腺癌发病率的逐年上升,精准诊断与分层治疗成为改善患者预后的关键。多...[详细]
-
带状疱疹神经疼痛的临床诊疗
综合治疗的必要性带状疱疹神经痛的治疗需要多模式、多学科的综合治疗策略。结合...[详细]

